كيف تتكون البحيرات الحمضية
تتكون الأمطار الحمضية من تفاعل الغازات المحتوية على الكبريت. وأهمها ثاني أكسيد الكبريت مع الأكسجين بوجود الأشعة فوق البنفسجية الصادرة عن الشمس، وينتج ثالث اكسيد الكبريت الذي يتحد بعد ذلك مع بخار الماء الموجود في الجو، ليعطي حمض الكبريت.
كيف يتكون المطر الحمضي
المطر الحمضي هو مطر أو أي نوع من الهطول يحتوي على أحماض. الأمطار الحمضية لها تأثيرات مدمرة على النباتات والحيوانات المائية. معظمها تتكون بسبب مركبات النيتروجين والكبريت الناتجة عن الأنشطة البشرية والتي تتفاعل في الجو لتكوّن الأحماض. وضعت الكثير من الحكومات في السنوات الأخيرة بعض القوانين التي تحد من إنتاج هذه المركبات المسببة للأمطار الحمضية.
المصدران الرئيسيان للمطر الحامض هما ثاني اكسيد الكبريت (SO2) واكسيد النيتروجين (NO2).
إن هذه الغازات منتجات ثانوية لعمليات احتراق بدرجات حرارة عالية (دخان السيارات والمصانع وحرق الغابات) والصناعات الكيماوية مثل إنتاج الأسمدة. وتشكل العمليات الطبيعية مثل تأثير البكتيريا على التربة وحرائق الغابات والنشاط البركاني والبرق 5 في المائة من اكسيد النيتروجين المنبعث، أما المواصلات فتشكل 43 في المائة بينما تشكل عمليات الاحتراق الناجمة عن المصانع 32 في المائة.
ثاني أكسيد الكبريت
ينبعث ثاني أكسيد الكبريت (غاز عديم اللون) كمنتج ثانوي ناجم عن الوقود الاحفوري المحترق الذي يحتوي على الكبريت. وينتج هذا الغاز عن عدة عمليات صناعية مثل إنتاج الحديد والصلب والمصانع وعمليات تصنيع النفط الخام.
ويمكن أن ينبعث ثاني أكسيد الكبريت في الجو نتيجة للكوارث الطبيعية، ويشكل هذا 10% من مجموع هذا الغاز المنبعث من البراكين ورذاذ ماء البحر والعوالق (الكائنات الحية المعلقة في الماء) والنباتات المتعفنة. وعلى العموم فإن 69,4 في المائة من ثاني اكسيد الكبريت ينتج عن الاحتراق الصناعي. أما المواصلات فهي مسؤولة عن 3,7 في المائة من ثاني اكسيد الكبريت المنبعث.
ثاني أكسيد النيتروجين
أما المادة الكيماوية الأخرى المسؤولة بشكل رئيسي عن تكوين المطر الحمضي فهي أكسيد النيتروجين، وتستخدم هذه العبارة لوصف أي مركب من النيتروجين مع أية كمية من ذرات الأكسجين. ان أول اكسيد النيتروجين وثاني اكسيد النيتروجين هما الاثنان أكسيدا نيتروجين.
تطلق عبارة المطر الحامض على الأمطار التي يكون معدل الأس الهيدروجيني فيها أقل من 5,6 (<5,6) إذ يعتبر معدل PH=7 متعادلا.
ويدور حاليا جدل شديد بالنسبة إلى هذا النوع من تلوث الهواء بسبب الضرر الذي يلحقه بالبيئة والممتلكات في العالم. ففي السنوات العشر الماضية تسببت هذه الظاهرة في تدمير آلاف البحيرات والجداول المائية في الولايات المتحدة وكندا ومناطق أخرى في أوروبا.
ويعتبر غاز اكسيد النيتروجين خطيرا في حد ذاته إذ انه يهاجم أغشية أعضاء الجهاز التنفسي ويزيد من احتمال الإصابة بالأمراض التنفسية، كما يساهم في اتلاف طبقة الأوزون ويعمل على تكوين الضباب الدخاني. ويمكن أن ينتشر الاكسيد بعيدا عن المكان الذي تكون فيهِ بواسطة المطر الحامض. وتعمل التغييرات البيئية على تغيير الحياة البرية الموجودة في المناطق التي حدث فيها التغيير.
تكون الأمطار الحمضية
تتكون الأمطار الحمضية من تفاعل الغازات المحتوية على الكبريت. وأهمها ثاني أكسيد الكبريت مع الأكسجين بوجود الأشعة فوق البنفسجية الصادرة عن الشمس، وينتج ثالث اكسيد الكبريت الذي يتحد بعد ذلك مع بخار الماء الموجود في الجو، ليعطي حمض الكبريت.
الذي يبقى معلقا في الهواء على هيئة رذاذ دقيق تنقله الرياح من مكان لآخر، وقد يتحد مع بعض الغازات في الهواء مثل النشادر، وينتج في هذه الحالة مركب جديد هو كبريتات النشادر، أما عندما يكون الجو جافا، ولا تتوفر فرصة لسقوط الأمطار، فان رذاذ حمض الكبريت، ودقائق كبريتات النشادر تبقى معلقة في الهواء الساكن، وتظهر على هيئة ضباب خفيف، لاسيما عندما تصبح الظروف مناسبة لسقوط الأمطار فإنهما يذوبان في ماء المطر، ويسقطان على سطح الأرض على هيئة مطر حمضي، وتشترك اكاسيد النيتروجين مع اكاسيد الكبريت في تكوين الأمطار الحمضية حيث تتحول أكاسيد النيتروجين بوجود الأكسجين والأشعة فوق البنفسجية إلى حمض النيتروجين.
ولابد من إبداء الملاحظتين الآتيتين في هذا المجال:
الملاحظة الأولى: ان الغازات الملوثة تنتقل بواسطة التيارات الهوائية تؤكد الدراسات في إسكندنافيا ان كمية غازات الكبريت أعلى (2.0) مرة مما تطلقه مصانعها، وفي الوقت نفسه، لا تزيد كمية غازات الكبريت في اجواء بعض اقطار أوروبا الغربية، وخاصة المملكة المتحدد عن 10- 20%. وهذا يعني ان هذه الغازات الملوثة، تنتقل بواسطة التيارات الهوائية من أوروبا الغربية إلى إسكندنافيا وإنكلترا.
الملاحظة الثانية: الأمطار تزداد مع الزمن، كما جاء في كتاب “التلوث مشكلة العصر” حيث تشير الدراسات إلى ان حموضة الأمطار التي سقطت فوق السويد عام 1982 كانت أعلى بعشر مرات من حموضة الأمطار التي سقطت عام 1969، حيث لاحظ الخبراء أن نسبة حموضة مياه الأمطار زادت بشكل منذر بالخطر، أما درجة حموضة الأمطار في بريطانيا فقد وصلت إلى 4.5 في عام 1979، ووصلت في نفس العام في كندا إلى 3.8 وفي فرجينيا إلى 1.5، حيث كانت درجة حموضة أمطار فرجينيا تقارب درجة حموضة حمض الكبريت (حامض البطارية) وفي اسكتلندا، وصلت إلى 2.7 عام 1977، ووصلت في لوس أنجلس إلى 3 عام 1980. اي أكثر حموضة من الخل وعصير الليمون.
ولا يقتصر التوزع الجغرافي للأمطار على البلاد الصناعية، إذ يمكن ان تنتقل الغيوم لمسافات بعيدة عن مصادر التلوث الصناعي، فتهطل أمطارا حمضية على مناطق لا علاقة لها بمصدر التلوث. ولابد من الإشارة إلى ان درجة حموضة ماء المطر النقي هي بين 5.5 – 6 اي تميل إلى الحموضة قليلا، ولم يسجل أي تأثير سلبي لهذه النسبة حصل خلال ملايين السنين، ويمكن اعتبار ماء المطر نقيا في حدود هذه الدرجة وغير ضار بالبيئة حسب المعلومات المتوفرة.
الأمطار الحمضية ومخاطرها البيئية
تعد الأمطار الحمضية من أخطر الظواهر الطبيعية تدميراً للبيئة وإضراراًً بصحة الإنسان، فعندما تسقط هذه الأمطار علي الغابات والمناطق الزراعية فإنها تؤدي إلي هلاكها، مثلما حدث في غابات “أور” في تشيكوسلوفاكيا، حيث أدي المطر الحمضي إلي القضاء علي نحو خمسين ألف هكتار من هذه الغابات.
وإذا ما سقطت هذه الأمطار على المحيطات والبحار والأنهار، فإنها تتسبب في إصابة الكائنات البحرية بأضرار جسيمة، كما يتفاعل الماء الحمضي مع رصاص ونحاس مواسير المياه، ويلوث مياه الشرب، فيدمر الكبد والكلى، ويؤدي أيضاً إلى تآكل المنشآت الحجرية والأبنية الأثريّة القديمة، مثلما حدث لبعض أحجار برج لندن وكنيسة لودستمتستر، حيث بلغ عمق التآكل بضع سنتيمترات نتيجة التفاعل بين غاز ثاني أكسيد الكبريت والأمطار التي تسقط من حين لآخر.
وقد كان الاعتقاد السائد أن الأمطار الحمضية، تنشأ نتيجة بعض العوامل الطبيعية التي لا دخل للإنسان فيها، مثـل الغازات الحمضية الناجمة عن اندفاع البراكين، أو من حرائق الغابات، أو من تحلل بقايا النباتات والحيوانات، لكن العلم الحديث كشف أن السبب الرئيسي للأمطار الحمضية هو النشاط البشري، وأوضحت الدراسات أن 90% من الكبريت المحمول في الأمطار يرجع إلى دخان المصانع ومحطات إنتاج الطاقة الكهربائية، ونتيجة حرق الفحم والبترول بكميات كبيرة، حيث ينتج عن احتراقهما ثاني أكسيد الكبريت.
ويكتسب المطر الصفة الحمضية، نتيجة تفاعل الغازات المحتوية علي الكبريت و ثاني أكسيد الكربون مع أكسجين الهواء في وجود الأشعة فوق البنفسجية الصادرة من الشمس، فتتحول إلي ثاني وثالث أكسيد الكبريت الذي يتحد بعد ذلك مع بخار الماء الموجود في الغلاف الجوي ليعطي حمضاً قوياً يعرف باسم حمض الكبريتيك، ويبقي حمض الكبريتيك المتكون معلقاً في الهواء علي هيئة رذاذ دقيق تتناقله الرياح من مكان لآخر.
وقد يتحد هذا الحمض مع بعض المواد القلوية التي توجد في الهواء مثل النشادر وينتج عن ذلك كبريتات النشادر، وحينما تصبح الظروف مواتية لسقوط الأمطار، فإن هذا الحمض يذوب في ماء المطر الذي يسقط علي الأرض في شكل مطر حمضي.
ويتوقف تأثير الأمطار الحمضية على عدد من العوامل مثل كمية الأمطار المتساقطة والفترة الزمنية التي يستغرقها هطول المطر الحمضي، ومستوى حموضة الأمطار والتركيب الكيماوي للتربة والنباتات والمياه الطبيعية، ومدى تأثر النباتات والحيوانـات والمنشآت بحموضـة الأمطار وحرارة الجو، ووجود ملوثات أخرى في الهواء وما إلى ذلك.
وتؤدي الأمطار الحمضية إلى إذابة نسبة كبيرة من الفلزات الثقيلة مثل الرصاص والزئبق والألمنيوم، وهي فلزات سامة وتسبب تسمم الكائنات الحية عند شربها للمياه الملوثة.
كما تتصف بخاصية التراكم، حيث تتجمع بمرور الوقت فـي أجسام الأحياء، وقد لوحظ انخفاض أعداد الطيور في بعض المناطق الأوربية والأمريكية نتيجة تغذيها على الحشرات التي تحتوي أجسامها على نسبة عالية من الألمنيوم التي جرفته مياه الأمطار الحمضية من سطح التربة وحملته إلى الماء.
وقد كشفت الدراسات أن الأمطار الحمضية تتسبب في تدمير وانقراض الآلاف من الكائنات الحية البحرية، وتؤدي إلى موت القشريات والضفادع والأسماك الصغيرة، بسبب تكون مركبات سامة بتأثير حموضة الأمطار، تتركز في أنسجتها فتتسبب في وفاتها.
وتتأثر البحيرات والمحيطات وما تحتويه منن ثروات بحرية سلباً بالأمطار الحمضية، من خلال انتقال حمض الكبريتيك إليها مع مياه السيول والأنهار بعد هطول الأمطار الحمضية، كما أن الأمطار الحمضية تجرف معها عناصر معدنية مختلفة بعضها على شكل مركبات من الزئبق والرصاص والنحاس والألمنيوم، مما يتسبب في قتل الكثير من الكائنات الحية البحرية.
ودرجة الحموضة الطبيعية لمياه البحيرات تتراوح بين 5- 6 درجات، فإذا زادت عن ذلك، ظهرت المشاكل البيئية. وتشير الإحصائيات إلى أن عدد البحيرات التي زادت نسبة حموضتها على مستوى العالم ارتفع بصورة غير مسبوقة ليصل إلى نحو ثلث البحيرات الموجودة حالياً، والتي أدت الأمطار الحمضية إلى نوع من الخلل البيئي واضطراب الحياة فيها.
كذلك فإن الأمطار الحمضية تدمر الغابات والأراضي الزراعية، فهي تجرد الأشجار من أوراقها، و تذيب بعض المعادن أو الفلزات الهامة وتبعدها عن جذور النبات، مثل الكالسيوم والبوتاسيوم والمغنيسيوم التي تجرفها مياه الأمطار الحمضية بعيداً عن جذور النباتات إلى المياه الجوفية، وبذلك تقل جودة المحاصيل الزراعية، كما تحدث الأمطار الحمضية خللاً في التربة، فتؤدي إلى اضطراب عملية الامتصاص في الجذور، مما يؤثر سلباً على الإنتاجية.
وتتأثر معظم الغابات في شرقي الولايات المتحدة الأمريكية، بالأمطار الحمضية، وتصيبها حالة تسمى “فالدشترين” وتعني موت الغابة، وأكثر الأشجار تأثرا بالأمطار الحمضية هي أشجار الصنوبر، نظرا لسقوط أوراقها قبل موعدها، وهو ما يؤدي إلى فقدان الأخشاب لجودتها، ويتسبب في خسارة اقتصادية كبيرة، نتيجة تدمير الغابات وتدهور إنتاجيتها.
وتؤثر الأمطار الحمضية أيضاً على التربة الزراعية، فتؤدي إلى انخفاض نشاط البكتيريا المثبتة للنيتروجين. وتراجع معدل تحلل المواد العضوية، مما يترتب عليه زيادة حجم البقايا النباتية، على نحو يعوق نفاذ الماء إلى داخل التربة، ويحول دون إنبات البذور، وهذه التأثيرات السلبية تؤدي إلى انخفاض إنتاجية الغابات والأراضي الزراعية.
وتتسبب الأمطار الحمضية كذلك في أضرار صحية كبيرة للإنسان، ومن ذلك احتقان الأغشية المخاطية وتهيجها وكذلك السعال والاختناق وتلف الأنسجة، وذلك حينما يتشكل الضباب الدخاني، لاسيما في المدن الكبيرة، وهو يحتوي على حموضة مرتفعة، ويبقى معلقاً في الجو عدة أيام، ويرجع تكون ذلك الضباب الحمضي إلى تعرض الملوثات الناتجة عن وسائل النقل إلى الأشعة فوق البنفسجية الآتية من الشمس، فتحدث بين مكوناتها تفاعلات كيميائية تؤدي إلى تكوين الضباب الدخاني الذي يخيم على المدن، وخاصة في الساعات الأولى من الصباح.
وقد أظهرت الدراسات التي أجريت على الضباب الحمضي أنه أكثر خطورة من المطر الحمضي، على الرغم من أنهما يتكونان بطريقة واحدة، ويرجع ذلك إلى أن الضباب الحمضي يتكون ويتكثف بالقرب من سطح الأرض، وبذلك تصبـح الفرصة مهيأة لإحداث أضرار بالغة بالذين يستنشقونه.ولا يقتصر تأثير الضبـاب الحمضي على الإنسان فحسب، بل يمتد ليشمل النباتات والحيوانات والمباني الأثرية.
وللحد من مشكلة الأمطار الحمضية، فإنه يجب معالجة أسبابها، بالحد من إحراق الوقود داخل المصانع ومحطات توليد الطاقة ووسائل المواصلات، واستخدم أفران ومواقد جديدة تقلل من انطلاق كل من أكاسيد الكبريت وأكاسيد النيتروجين. واستخدام محطات التكرير الحديثة التي تنتج نفطاً يحتوي على نسبة منخفضة من الكبريت، أو تنظيف معظم أنواع الفحم الحجري الموجود فيه، وذلك عن طريق استخدام السحق، بواسطة بعض العمليات الكيميائية.
ويمكن إتباع بعض الطرق لتقليل أخطار الأمطار الحمضية، ومن ذلك طلاء المنشآت والمباني والآثار بأنواع مستحدثة من الطلاء لحمايتها من الآثار الضارة لسقوط الأمطار الحمضية عليها، واستخدام الجير في معالجة البحيرات التي تتعرض للأمطار الحمضية، حيث يتسبب الجير في معالجة حموضة المياه، ويتم ذلك عن طريق رش رذاذ من الجير على سطح الماء من زوارق خاصة تطوف بكل أرجاء البحيرة لغرض معالجة مياهها.
ولكن عيب هذه الطريقة أنها مكلفة للغاية، كما أنها تحتاج إلى عناية كبيرة ودقة فائقة في استخدام الجير حتى لا تنقلب الحالة في تحول مياه البحيرات في حالة الحموضة إلى الحالة القلوية.
(بالإنجليزية: Acid rain) هو مطر أو أي نوع من الهطول يحتوي على أحماض لمطر الحِمْضِي هو المطر الذي يكتسب الصِّفَة الحِمْضِيّة. وتحدث الأمطار الحِمْضِيّة عندما تتفاعل أكاسِيْد الكبريت والنتروجين المنبعِثَة من ملوِّثات مختلفة، مع بخار الماء في الجو؛ لتتحوّل إلى أحماض ومركّبات حِمْضِيّه ذائبة، وتبقى عَالِقة في الهواء حتى تتساقط مع مياه الأمطار.
الغَازَات التي تؤدي إلى تكون المطر الحِمْضِي:
1- غاز ثاني أُكْسيد الكبريْتِيْد.
2- أكاسِيْد النيتروجِيْن.
3- ثاني أكْسيد الكربون.
4- الكلوْر.
التَّرْسِيْب الحِمْضِي الجاف:
في بعض المناطق التي لا تسقط فيها الأمطار، تلتصِق هذه المركبات الحمضيّة بالأتربة العَالِقَه في الهواء، وتتساقط معها لتلْتَصِقَ بسطح التربة. وتسمى هذه الظاهرة بالترْسِيْب الحِمْضِي الجاف. ثم تأتي الرياح وتحمل هذه الذَّرَّات الترابيّة الحِمْضِيَّة وترسِّبُها على المباني، والسّيّارات، والمنازل، والأشجار، ثم تنزل الأمطار لتغْسِلَ هذه الأسطح؛ فتتحول الأمطار إلى أمطار حِمْضِيّة بدرجة أكثر.
تأْثير المطر الحِمْضِى:
* يزيد من حِمْضِيّة مياه الأنهار والينابيع والبُحَيْرات، ويضر بالتربة والحياة النباتية، ويتلف الأبنية، وخاصة الأثريّة القديمة.
* يحلِّلُ بعض مركّبات المعادن السّامّة الموجودة على سطح التربة، لتصبح حرة؛ فيتركز بعضها في الأنهار- المصدر الأساسي لمياه الشرب لمعظم شعوب العالم-، مثل الزِّئْبق الذي يتخلل جلود الأسماك؛ فتضر بصحة الإنسان الذي يأكلها.
* يتفاعل الماء الحِمْضِي مع رصاص ونحاس مواسير المياه، ويلوِّث مياه الشّرب؛ فيُدمّر الكَبِدَ والكُلَى
معادلة تكوين المطر الحمضي
تعتمد العديد من الأنشطة البشرية على حرق كميات كبيرة من الوقود الاحفوري، ممّا يؤدّي إلى انبعاث غازات، مثل: ثاني أكسيد الكبريت (SO2)، وأكاسيد النيتروجين (NOX)، والتي تُساهم بشكل كبير في تكوين المطر الحمضي، إذ تتفاعل هذه الغازات مُنتجةً أحماض النيتريك والكبريتيك التي تعدّ المكوّن الأساسي له، ويبيّن ما يأتي بعض التفاعلات الكيميائية التي تحدث في الغلاف الجوي مكوّنة المطر الحمضي: تفاعلات ثنائي أكسيد الكبريت (SO2) في الحالة الغازية: ينتُج غاز ثنائي أكسيد الكبريت عن طريق تفاعل الكبريت المُنبعث من احتراق الفحم مع جزيء الأكسجين، وذلك عبر التفاعل الآتي: (S (g) + O2 (g) → SO2 (g فيما بعد، يتفاعل غاز ثنائي أكسيد الكبريت مرّة أخرى مع جزيء الأكسجين لإنتاج ثلاثي أكسيد الكبريت، وذلك عبر التفاعل الآتي: (2SO2 (g) + O2 (g)→ SO3 (g ثمّ تتفاعل أشعة الشمس مع جذر الهيدروكسيل وثنائي أكسيد الكبريت لإنتاج حمض الكبريتيك، وذلك عبر التفاعل الآتي: (SO2 (g) + 2(OH) (g) → H2SO4 (g تفاعلات ثنائي أكسيد الكبريت (SO2) في الحالة السائلة: يتفاعل ثلاثي أكسيد الكبريت مع بخار الماء الموجود في الغلاف الجوي لإنتاج حمض الكبريتيك، وذلك عبر التفاعل الآتي: (SO3 (g) + H2O (l) → H2SO4 (l تفاعلات أكاسيد النيتروجين (NOX) في الحالة الغازية: تمزج محرّكات الاحتراق الأكسجين مع النيتروجين بوجود الطاقة لإنتاج أحادي أكسيد ثنائي النيتروجين، وذلك عبر التفاعل الآتي: (g) N2 (g) + O2 (g) + Energy → 2NO فيما بعد، يتفاعل أحادي أكسيد ثنائي النيتروجين مع جزيء الأكسجين ثنائي الذرة لإنتاج ثنائي أكسيد النيتروجين، وذلك عبر التفاعل الآتي: 2NO (g) + O2 (g) → 2NO2 (g) ثمّ تتفاعل اشعة الشمس مع جذر الهيدروكسيل وثنائي أكسيد النيتروجين لإنتاج حمض النيتريك، وذلك عبر التفاعل الآتي: (NO2 (g) + OH (g) → HNO3 (g تفاعلات أكاسيد النيتروجين (NOX) في الحالة السائلة: يتفاعل ثنائي أكسيد النيتروجين مع بخار الماء الموجود في الغلاف الجوي لإنتاج حمض النيتريك، وذلك عبر التفاعل الآتي: (NO2 (g) + H2O (l) → HNO3 (l
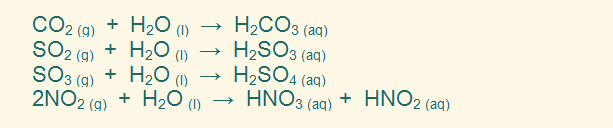
مكونات المطر الحمضي
مكوّنات المطر الحمضي تتكوّن الأمطار الحمضية من مزيج من أحماض النيتريك (HNO3) والكبريتيك (H2SO4)، والتي تنتج من تفاعل انبعاثات ثاني أكسيد الكبريت (SO2) وأكاسيد النيتروجين (NOX) المُتصاعدة عبر تيارات الهواء والرياح في الغلاف الجوي مع كلّ من الماء، والأكسجين، والمركبات الكيميائية الأخرى، إذ تختلط أحماض النيتريك والكبريتيك فيما بعد مع الماء، وتسقط على شكل أمطار حمضية على الأرض، ويُمكن توضيح تلك التفاعلات من خلال المعادلات الكيميائية الآتية: تفاعل ثاني أكسيد الكبريت لإنتاج حمض الكبريتيك: SO2 + H2O → H2SO4 H2SO4 →← H+ + HSO4- →← 2H+ + SO4-2 تفاعل أكاسيد النيتروجين لإنتاج حمض النيتريك: NO2 + H2O → HNO3 -HNO3→ H+ + NO3 يُعدّ الماء النَّقي مادةً مُتعادلة، فهو ليس حمضياً ولا قاعدياً، إذ تعادل قيمة الرقم الهيدروجيني (PH) له 7، في حين يتراوح الرقم الهيدروجيني للأمطار النظيفة في الأوضاع الطبيعية ما بين 5.0-5.5، ممّا يعني أنَّ الأمطار العادية حمضية قليلاً، بينما يصل الرقم الهيدروجيني للأمطار الحمضية إلى 4، ويعني انخفاض الرقم الهيدروجيني من 5 إلى 4 أنَّ الحموضة ازدادت بمقدار عشرة أضعاف.
أسباب المطر الحمضي
تتعدد الأسباب المؤدية لتشكّل الأمطار الحمضية، حيث تلعب الأنشطة الحضارية دورًا هامًا في زيادة الملوثات الجوية الناتجة عن حرق الوقود الأحفوري والمخلفات البشرية
ولا يعد الإنسان المسؤول الوحيد عن تشكل الأمطار الحمضية، إذ تعدّ الكوارث الطبيعية عاملًا أيضًا، حيث تعد البراكين مثالًا واضحًا للكوارث الطبيعية الملوثة، تعمل على إطلاق الملوثات بكميات كبيرة نحو الجو خصوصًا المُركبات المحتوية على الكبريت.
ويعد ثاني أكسيد الكبريت (SO2) وأكاسيد النيتروجين (NOx) المنطلقين في الهواء، والناتجين من محطات الطاقة التي تعمل بالوقود الأحفوري ووسائل النقل والمركبات ومصافي النفط، السبب الأكبر للأمطار الحمضية اليوم، وفقًا لوكالة حماية البيئة.
كيف يتشكل المطر الحمضي؟
يختلط ثاني أكسيد الكبريت وأكاسيد النيتروجين مع الماء والأكسجين والمواد الكيميائية الأخرى في الغلاف الجوي محدثةً تفاعلًا كيميائيًا تتحول خلالها الأكاسيد لأحماض الكبريتيك والنتريك التي تختلط بدورها مع مياه الأمطار مشكلة ما يسمى بالمطر الحمضي.
تأثيرات المطر الحمضي
يؤثر المطر الحمضي على كل شيء تقريبًا، خاصّة الإنسان والبيئات الحيوية المختلفة، إضافًة لامتداد تأثيره للمباني والمنشآت العمرانية والتماثيل
وتعد البيئات المائية، مثل الجداول والبحيرات والمستنقعات والبحار وغيرها، الأكثر تضررًا بالأمطار الحمضية ، إذ تعمل على تغييّر تركيبتها، ، ما قد يُضر بالأسماك والكائنات المائية وغيرها من الحيوانات البرية الأخرى.
ويحتوي المطر الحمضي على النيتروجين الذي يسبب تلوثًا جزئيًا في المياه الساحلية مما يتسبب في انخفاض أعداد الأسماك والمحاريات في تلك المناطق.
ويعمل المطر الحمضي على ترشيح الألومنيوم من التربة، والذي يعد عنصرًا ضارًا للنباتات والحيوانات.
كما تزيل هذه الأمطار المعادن والمواد المغذية التي تحتاجها الأشجار للنمو من التربة.
وتعد الأشجار الميتة من المشاهد الشائعة في المناطق المتضررة بالأمطار الحمضية، إضافًة لإضعاف قدرة الأشجار الموجودة على تحمل درجات حرارة التجمد في المناطق المرتفعة، حيث يُجرّد الأوراق من العناصر الغذائية وبالتالي تصبح الأشجار أقل قدرة على امتصاص أشعة الشمس.
ويتسبب الترسيب الجاف في إتلاف أسطح التماثيل والمباني وغيرها من الهياكل التي يصنعها الإنسان. إذ يؤدي إلى تدهور الطلاء والحجر بسرعة أكبر وتلّوث أسطح المباني والهياكل الأخرى مثل الآثار بالغبار.
وعواقب هذا الضرر ، يُمكن أن تكون مكلفة حيث تحتاج المواد التالفة إلى إصلاح أو استبدال مما يزيد من تكاليف الصيانة، وفقدان التفاصيل على التماثيل الحجرية والمعادن والمعالم الأثرية وشواهد القبور.
ويؤثر المطر الحمضي على صحة الإنسان وأعضائه الحيوية، فقد يتفاعل ثاني أكسيد الكبريت وأكسيد النيتروجين في الغلاف الجوي لتكوين جسيمات كبريتات ونترات دقيقة تصل إلى الرئتين عبر التنفس.
وأظهرت العديد من الدراسات العلمية وجود علاقة بين هذه الجزيئات والتأثيرات على وظائف القلب، مثل النوبات القلبية، إضافًة للتأثيرات على وظائف الرئة، مثل صعوبة التنفس للأشخاص الذين يعانون من الربو.
أضرار الأمطار الحمضية
المشاكل البيئية. وتشير الإحصائيات إلى أن عدد البحيرات التي زادت نسبة حموضتها على مستوى العالم ارتفع بصورة غير مسبوقة ليصل إلى نحو ثلث البحيرات الموجودة حالياً، والتي أدت الأمطار الحمضية إلى نوع من الخلل البيئي واضطراب الحياة فيها.
كذلك فإن الأمطار الحمضية تدمر الغابات والأراضي الزراعية، فهي تجرد الأشجار من أوراقها، و تذيب بعض المعادن أو الفلزات الهامة وتبعدها عن جذور النبات، مثل الكالسيوم والبوتاسيوم والمغنيسيوم التي تجرفها مياه الأمطار الحمضية بعيداً عن جذور النباتات إلى المياه الجوفية، وبذلك تقل جودة المحاصيل الزراعية، كما تحدث الأمطار الحمضية خللاً في التربة، فتؤدي إلى اضطراب عملية الامتصاص في الجذور، مما يؤثر سلباً على الإنتاجية.
وتتأثر معظم الغابات في شرقي الولايات المتحدة الأمريكية، بالأمطار الحمضية، وتصيبها حالة تسمى “فالدشترين” وتعني موت الغابة، وأكثر الأشجار تأثرا بالأمطار الحمضية هي أشجار الصنوبر، نظرا لسقوط أوراقها قبل موعدها، وهو ما يؤدي إلى فقدان الأخشاب لجودتها، ويتسبب في خسارة اقتصادية كبيرة، نتيجة تدمير الغابات وتدهور إنتاجيتها.
وتؤثر الأمطار الحمضية أيضاً على التربة الزراعية، فتؤدي إلى انخفاض نشاط البكتيريا المثبتة للنيتروجين. وتراجع معدل تحلل المواد العضوية، مما يترتب عليه زيادة حجم البقايا النباتية، على نحو يعوق نفاذ الماء إلى داخل التربة، ويحول دون إنبات البذور، وهذه التأثيرات السلبية تؤدي إلى انخفاض إنتاجية الغابات والأراضي الزراعية.
وتتسبب الأمطار الحمضية كذلك في أضرار صحية كبيرة للإنسان، ومن ذلك احتقان الأغشية المخاطية وتهيجها وكذلك السعال والاختناق وتلف الأنسجة، وذلك حينما يتشكل الضباب الدخاني، لاسيما في المدن الكبيرة، وهو يحتوي على حموضة مرتفعة، ويبقى معلقاً في الجو عدة أيام، ويرجع تكون ذلك الضباب الحمضي إلى تعرض الملوثات الناتجة عن وسائل النقل إلى الأشعة فوق البنفسجية الآتية من الشمس، فتحدث بين مكوناتها تفاعلات كيميائية تؤدي إلى تكوين الضباب الدخاني الذي يخيم على المدن، وخاصة في الساعات الأولى من الصباح.
وقد أظهرت الدراسات التي أجريت على الضباب الحمضي أنه أكثر خطورة من المطر الحمضي، على الرغم من أنهما يتكونان بطريقة واحدة، ويرجع ذلك إلى أن الضباب الحمضي يتكون ويتكثف بالقرب من سطح الأرض، وبذلك تصبـح الفرصة مهيأة لإحداث أضرار بالغة بالذين يستنشقونه.ولا يقتصر تأثير الضبـاب الحمضي على الإنسان فحسب، بل يمتد ليشمل النباتات والحيوانات والمباني الأثرية.
وللحد من مشكلة الأمطار الحمضية، فإنه يجب معالجة أسبابها، بالحد من إحراق الوقود داخل المصانع ومحطات توليد الطاقة ووسائل المواصلات، واستخدم أفران ومواقد جديدة تقلل من انطلاق كل من أكاسيد الكبريت وأكاسيد النيتروجين. واستخدام محطات التكرير الحديثة التي تنتج نفطاً يحتوي على نسبة منخفضة من الكبريت، أو تنظيف معظم أنواع الفحم الحجري الموجود فيه، وذلك عن طريق استخدام السحق، بواسطة بعض العمليات الكيميائية.
ويمكن إتباع بعض الطرق لتقليل أخطار الأمطار الحمضية، ومن ذلك طلاء المنشآت والمباني والآثار بأنواع مستحدثة من الطلاء لحمايتها من الآثار الضارة لسقوط الأمطار الحمضية عليها، واستخدام الجير في معالجة البحيرات التي تتعرض للأمطار الحمضية، حيث يتسبب الجير في معالجة حموضة المياه، ويتم ذلك عن طريق رش رذاذ من الجير على سطح الماء من زوارق خاصة تطوف بكل أرجاء البحيرة لغرض معالجة مياهها.
ولكن عيب هذه الطريقة أنها مكلفة للغاية، كما أنها تحتاج إلى عناية كبيرة ودقة فائقة في استخدام الجير حتى لا تنقلب الحالة في تحول مياه البحيرات في حالة الحموضة إلى الحالة القلوية.
علاج الأمطار الحمضية
إزالة الكبريت من غاز المداخن وعوادم السيارات.
تنظيم الانبعاثات الناتجة عن السيارات والمباني.
تقييد استخدام الوقود الأحفوري والتركيز على مصادر طاقة أكثر استدامة مثل الطاقة الشمسية وطاقة الرياح.
استخدام الحجر الجيري أو الجير liming)).
توعية وتثقيف الأفراد بطرق الحفاظ على الطاقة وتقليل الانبعاثات.
الإجراءات الوقائية الدولية ودور منظمات الحماية البيئية في التوعية والتثقيف.
إزالة الكبريت من غاز المداخن وعوادم السيارات.
تنظيم الانبعاثات الناتجة عن السيارات والمباني.
تقييد استخدام الوقود الأحفوري والتركيز على مصادر طاقة أكثر استدامة مثل الطاقة الشمسية وطاقة الرياح.
استخدام الحجر الجيري أو الجير liming)).
توعية وتثقيف الأفراد بطرق الحفاظ على الطاقة وتقليل الانبعاثات.
الإجراءات الوقائية الدولية ودور منظمات الحماية البيئية في التوعية والتثقيف.
الأمطار الحمضية واثرها على البيئة pdf
لتحميل الملف اضغط هنا









